



如何将药物直接“快递”到家(肿瘤细胞)呢?近日浙江大学化学工程与生物工程学院申有青教授团队和加州大学洛杉矶分校顾臻教授团队合作,提出了纳米药在肿瘤组织中主动渗透新机制,使纳米药在实体瘤渗透到每一个角落、将抗肿瘤药物输送到每一个肿瘤细胞,并用多种动物模型验证了这种方法能够显著提高抗肿瘤疗效。 这项研究刊登在国际知名期刊《自然·纳米技术》。
绕开“密林”为纳米药“改路”
“治疗癌症的纳米药,是将小分子抗肿瘤药负载到纳米尺寸的载体中得到的。”申有青介绍道,其直径在10—100纳米,是小分子药的几十倍,可称得上名副其实的“大象级药”。
据了解,相较于小分子药,纳米药的优势在于注射入血液后可以躲过肾脏过滤,在血液中滞留更长时间,从而能更多地蓄积在肿瘤中。囿于其“庞大”的体积,其自身扩散能力却很弱。
“肿瘤内部缺少毛细血管网,有非常致密的细胞外基质和非常高的细胞密度。”申有青说,纳米药在肿瘤组织内的扩散,犹如一只大象在枝蔓横生的原始密林中一样难以前行,导致纳米药即便能够积蓄在瘤内,也无法将携带的药物直接递送到每一个细胞内。
针对这一问题,国内外学者已通过利用降低肿瘤组织密度、减小纳米药尺寸等方法,来降低纳米药在瘤内的渗透阻力,但依然无法解决纳米药尺寸大、自身运动扩散能力弱、导致依靠自身扩散进行的瘤内被动渗透能力差等问题。
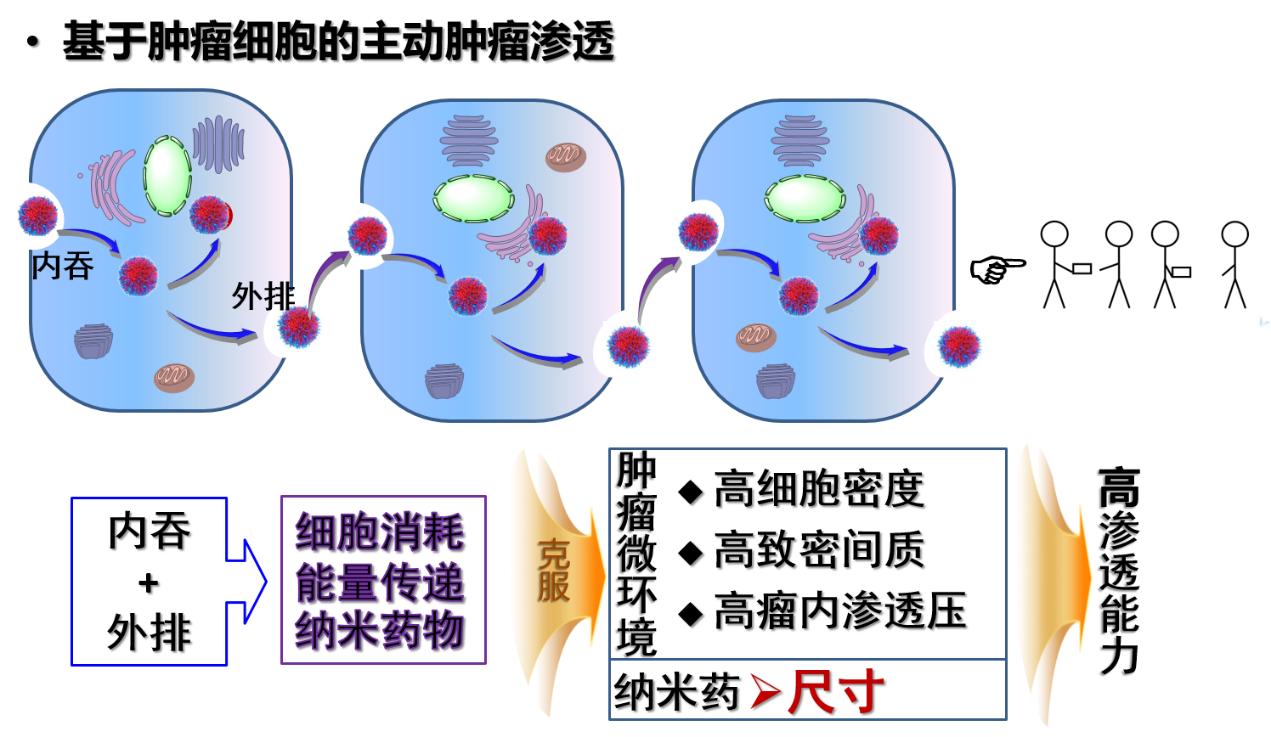
有没有可能发挥肿瘤细胞的“主动性”、让其“主动”地递送纳米药呢?这样既利用了瘤内高端细胞密度,又让纳米药直接在肿瘤细胞内穿行、绕开肿瘤细胞外基质这些“致密蔓藤”障碍。为此,申有青等设计了肿瘤细胞主动递送药物的方法:让肿瘤细胞一边吞噬纳米药,然后在另一边将一部分吐出来,这样循环往复,就将纳米药从肿瘤毛细血管处传递出去,到达每个肿瘤细胞。
这个过程的关键是细胞能够快速吞噬足够量的纳米药物,“细胞只有吃的够饱才会外排一些”。为此,申有青等利用正负电荷相吸原理。“肿瘤细胞表面带负电荷,因此带正电荷的纳米药很容易地被吸附到细胞表面而被内吞”,申有青介绍。本工作的关键设计之一是纳米药在血液中是电中性的,只有在肿瘤血管或肿瘤细胞附进才带上正电荷,来触发快速细胞内吞和主动肿瘤渗透。触发电中性向正电性转化的开关则是肿瘤血管的内皮细胞上及血管附近肿瘤细胞过表达的γ-谷氨酰转肽酶(GGT)。科研人员利用GGT响应性的基团来遮蔽正电荷;在肿瘤内GGT酶将修饰物去掉,使其呈现正电性。
吞吐之间,药物实现高效渗透
“细胞只有吃得够饱,才会外排一些药物。”据申有青介绍,纳米药在血液中原本呈现为电中性或电负性,需要使其在肿瘤血管或肿瘤细胞附近时快速呈正电性,才能让细胞吞噬足够量的纳米药物。
如何使药物在特定环境下快速“转性”,成了这场“接力赛”进行的关键。
“肿瘤血管的内皮细胞上及血管附近肿瘤细胞高表达的γ-谷氨酰转肽酶,成了我们将血液中药物向正电性转化的工具。”申有青表示,团队针对其在肿瘤细胞附近高表达的特点,设计合成了与其响应性的聚合物,可使药物达到肿瘤之后快速呈现正电性,进而完成跨细胞转运。
细胞内吞纳米药后,又如何让其“慷慨地”吐出一些?申有青说,这个“外排环节”,是细胞本身自带的功能,细胞中的高尔基体,就像是一个快递转运站,传递到高尔基体的物质会被打包外送出去。团队通过控制纳米药结构,使其被吞入后进入高尔基体,而非其他细胞器。
此次研究中,科研团队还用多种动物模型考察了该新结构的纳米药,结果表明尾静脉注射的纳米药可以治愈体积为100立方毫米的小肿瘤,同时能让500立方毫米的大肿瘤迅速萎缩变小,停药半个月后也未见明显反弹,抑瘤率高达98%。对于被称为癌症之王的“胰腺癌”,也有显著抑制其肿瘤生长的作用。
申有青表示,这种化被动渗透为主动的策略,克服了纳米药大尺寸导致扩散能力低的天然缺陷,有望解决纳米药在肿瘤组织内渗透难的问题,为下一阶段纳米药物的设计开辟了新思路。

