



3月18日,据西湖大学消息,该校研究团队首次揭开生命起始阶段“生命启动包”的核心密码,阐明了小RNA(核糖核酸)和CPL(细胞质晶格)在生命启程中的关键作用,为女性不孕、反复流产或胚胎停育等问题的研究提供新的思路。
据悉,西湖大学遗传物质表达与重构全国重点实验室申恩志团队接连在期刊《生命》(Vita)和《自然》(Nature)发表两项相关突破性研究。

研究团队合影
生命的起点始于精子与卵子的结合,受精初期胚胎依赖卵子中提前储备的母源蛋白和mRNA维持发育,如何精准调控这些“生命程序”,一直是该领域内未解之谜。
申恩志团队聚焦非编码小RNA与卵母细胞两大核心,历经近三年攻关,联合多个团队改进前沿技术,取得重大突破。
团队通过优化小RNA切割文库构建技术,绘制出小鼠卵母细胞内源性siRNA的靶向切割图谱,发现这类小RNA如同“分子剪刀”,在AGO2蛋白护送下,精准切断制造蛋白酶体关键零件的转录本,抑制其活性,避免其过度降解核糖体等生命关键“工厂”。
申恩志表示,研究团队意外发现,siRNA通路受损时,卵母细胞中占细胞质近10%的神秘纤维结构CPL会消失。这一60年前被发现的结构,其组成和功能真面目始终未知。
研究首次知道了CPL由哪些分子组成。分析结果显示,这是一套由14个蛋白质精密组装而成的超级结构。它的基本单元分为两种模块:“连接环”和“U型篮”。CPL还能把制造细胞骨架的关键材料——微管蛋白,也整合进来,变成自己的一部分。
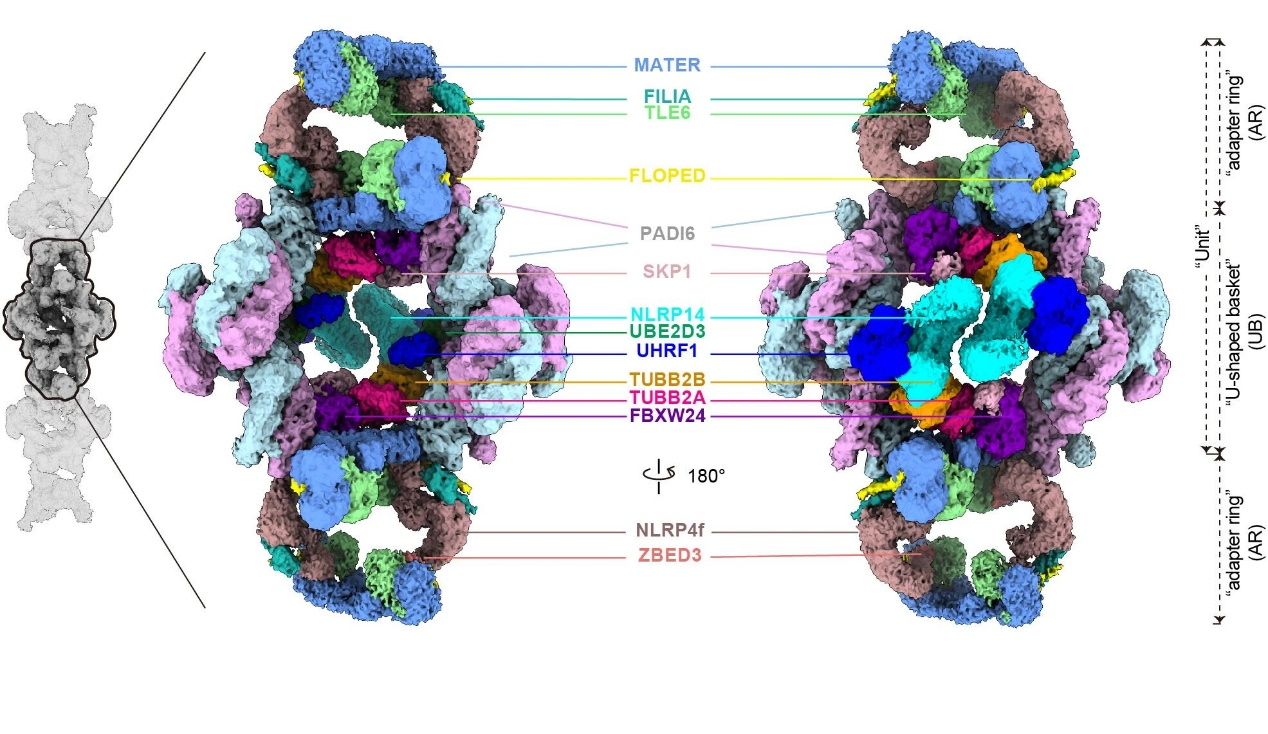
CPL的冷冻电镜结构
许多女性面临不孕、反复流产或胚胎停育的问题,往往找不到原因。研究显示,如果这条微小RNA通路出了问题,或者CPL结构不稳定,就可能导致胚胎在最早期就失败。据介绍,未来,医生或许可以通过检测这些分子标志物,提前预警风险,优化辅助生殖技术的成功率。